por Efraín Rincón
Los genes cargan las instrucciones de armado del rompecabezas de la vida. Determinan nuestra apariencia y características. Incluso, estos paquetes de información fijan qué tan susceptibles podemos ser a padecer una enfermedad. Recientes estudios han seguido las pistas en nuestros genes para ver por qué los efectos y la gravedad del COVID-19 son tan diferentes en las personas.
De la posibilidad de sobrevivir a reproducirse hay un largo trecho. En un ambiente donde hay depredadores acechando o las fuentes de alimento están condicionadas, vivir y no morir en el intento es todo un logro. Sin embargo, esa es solo una parte del trabajo, pues encontrar una pareja para dejar una descendencia es más significativo. Esa es la selección natural en acción, que Charles Darwin propuso en el siglo XIX, como el mecanismo para explicar la evolución de las especies.
En la teoría de la evolución por selección natural, una de las palabras claves es el rasgo, esa característica que es distinta entre individuos en una población, les da cierta “ventaja” a los que la poseen para sobrevivir y reproducirse y, muy importante, pasa de generación en generación, en otras palabras: se hereda.
Para cuando Darwin trabajaba en lo que hoy es una teoría que explica cómo cambian los organismos a través del tiempo, por qué se producen nuevas especies y qué quiere decir que compartamos con otros seres en este planeta un mismo ancestro, entender de qué manera un rasgo pasaba de una madre a un hijo era un misterio para el naturalista inglés. Incluso siendo contemporáneo durante varias décadas de Gregor Mendel A.K.A “el papá moderno de la genética”. Aunque a esta paternidad no se le dio el reconocimiento merecido sino mucho después.
Mendel, biólogo y monje austriaco, mientras experimentaba con arvejas, descubrió que los rasgos de estas plantas como el color o la rugosidad de sus semillas se heredaban. Claro, esto ya lo discernía Darwin, solo que Mendel se atrevió a ir más allá y explicó cómo ocurría. Por eso, sobre la herencia de rasgos, hoy podemos decir varias cosas. Por ejemplo, son ambos padres los que hacen aportes de información genética a su descendencia en forma de alelos (como que la semilla sea de color amarillo o verde). Además, estos alelos pueden ser dominantes, o sea que siempre se expresan en la descendencia, o recesivos, en otras palabras que aunque estén presentes, no se están expresando. Quizá un cuadrito como estos, los famosos cuadros de Punnett, les refresque la memoria.
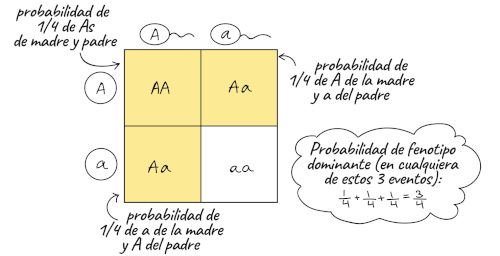
Este es un cuadro de Punnett que describe cómo serán los genotipos (alelos) y fenotipos (rasgos) de la descendencia y las probabilidades.
Tomado de Khan Academy
Al parecer, Mendel conocía del trabajo de Darwin, pero no al revés. Entonces, ¿qué hubiera pasado si el naturalista y el monje se hubieran enviado alguna carta, encontrado en un café o por casualidades de la vida topado en una calle? Probablemente las observaciones de Mendel hubieran servido de fundamento a la teoría de la evolución por selección natural de Darwin y, a cambio, la humanidad le hubiera dado la importancia que se merecía a los descubrimientos del austriaco. Solo hasta el siglo XX, gracias a verificaciones independientes de los principios de Mendel, se le dio el crédito que merecía y así empezó la genética moderna.

Los genes son el testigo que papás y mamás les pasan a las nuevas generaciones en esta carrera evolutiva de relevos. Son paquetes que contienen instrucciones necesarias para que la maquinaria celular de un organismo funcione. En nuestro caso, ellos determinan el color del pelo y los ojos, la altura y hasta la forma de las orejas, características físicas que son conocidas como fenotipos.
Sin embargo, esos no son los únicos fenotipos que nuestros genes ordenan. De hecho, las alteraciones en nuestra información genética, así sean muy pequeñas, podrían explicar por qué existe mayor susceptibilidad a enfermedades comunes como la diabetes, la hipertensión, el cáncer o la obesidad. También al COVID-19, como lo sugiere la evidencia más reciente. En medicina esto se conoce como susceptibilidad genética.
“Uno no se enferma de nada que no esté escrito en sus genes”, así lo expresa el doctor Ignacio Zarante, médico y genetista del Instituto de Genética Humana de la Universidad Javeriana. Aquí hay que dejar claro que la susceptibilidad está relacionada a la probabilidad, en este caso a la probabilidad de desarrollar una enfermedad. “Que esté ‘escrito’ en los genes no quiere decir que la persona se va a enfermar, pues se necesita de un ‘disparador’ para que eso se produzca”.
Nuestra información genética está escrita sobre mármol. El arreglo de letras en nuestro genoma literalmente nos determina —dime con qué genes andas y te diré quién eres— . Pero pese a que partimos de una base genética, la relación con el ambiente no la podemos obviar, este determina esos “disparadores” a los que se refiere Zarante. Un ejemplo es la relación que existe entre padecer cáncer de pulmón y el consumo de cigarrillo; en Estados Unidos el consumo de tabaco está asociado a cerca de entre el 80 % al 90 % de las muertes por cáncer de pulmón. Eso sí, hay quienes nunca han fumado o fuman poco y también desarrollan cáncer, o quienes fuman mucho y no desarrollan cáncer ¿por qué? Probablemente la respuesta última está en los genes. “Hay genes que me hacen susceptible a que yo tenga cáncer de pulmón”, dice este médico. Y fumar (nuestro ambiente) aumenta el riesgo de desarrollarlo.
Y así como la interacción que tenemos con nuestro entorno puede empeorar o aumentar el riesgo a padecer una enfermedad, también puede disminuirlo. Las probabilidades de sufrir de un ataque al corazón pueden ser menores con una dieta balanceada, haciendo ejercicio, evitando los cigarrillos, manteniendo un peso saludable, etc. Aunque exista una predisposición genética a sufrir un “ataque agudo del miocardio”, el riesgo de tenerlo depende del estilo de vida.
Los genes y las enfermedades infecciosas o ¿por qué hay gente que le va peor cuando se infectan con COVID-19?
¿Sabían que hay personas inmunes al virus responsable de la enfermedad del sida? Por lo menos un 10 % de la población europea puede no infectarse con el VIH. Y, otra vez, la respuesta está en sus genes. La evidencia indica que existe una mutación conocida como CCR5-delta 32 que evita la entrada del virus a las células —como si le pusiera “tranca” a la puerta que el virus utiliza para invadirnos—.
Y ojo, aquí les va un #DatoCoctelero: aparentemente las plagas virales de la Edad Media usaban el receptor CCR5 en la superficie de las células para invadir el sistema inmune. Como respuesta fortuita a esta presión que diezmaba a la población europea, apareció una mutación, sí, la CCR5-delta 32, que se mantuvo especialmente en la región escandinava y países como Rusia o Polonia. De hecho, es en esa parte del continente donde prevalece en mayor porcentaje la resistencia al VIH.
La frase del genetista ruso, Theodosius Dobzhansky, “nada tiene sentido en la biología si no es a la luz de la evolución”, cobra más significado que nunca. ¿Ya ven cómo la genética está en conversación tendida con el ambiente?
Y es el estudio de los genes que ahora nos ayuda a obtener pistas para entender un poco más al COVID-19. Recientemente, un estudio publicado en el New England Journal of Medicine ha sugerido una asociación entre unas regiones de nuestro genoma y el hecho de ser más vulnerables a esta enfermedad.
Según el equipo de investigadores, que analizó el genoma de 1.610 pacientes con COVID-19 en España e Italia, encontró que hay ciertas variaciones en un grupo de genes en una región del cromosoma 3. Estos genes, entre tanto, están relacionados con la producción de quimioquinas, señales químicas encargadas de reclutar células inmunológicas para que vayan a atacar a los patógenos. Una parte de las personas que se han infectado con este coronavirus han presentado una respuesta exagerada de estas células que termina por dañar los tejidos del propio cuerpo.
Los autores del estudio dicen que las alteraciones en estos genes afectan la regulación de estas quimioquinas. Además, un detalle no menos importante, los genes de esta región también están relacionados con la enzima convertidora de angiotensina 2 (ACE2), presente en varios tejidos del cuerpo, como los pulmones, y que son la cerradura que el coronavirus utiliza para entrar a nuestras células.
Otro hallazgo que muestran los resultados de esta investigación es que otra región de genes en el cromosoma 9, que determina el tipo de sangre, está asociada a un mayor o menor riesgo de sufrir de una falla respiratoria por COVID-19. En concreto, pacientes del tipo O tiene un riesgo menor frente a otros tipos de sangre distintos al O. Mientras que en pacientes del tipo A, el riesgo era mayor. “Pero esto no quiere decir que una persona A vaya a terminar en UCI si le da COVID-19. Solo tine un riesgo mayor”, recalca Zarante.
Estudios de este tipo se encaminan a buscar respuestas al porqué de la predisposición genética y su efecto en que ciertas personas tengan mayor riesgo de sufrir consecuencias más o menos graves por el COVID-19. También, eventualmente, a encontrar medicamentos que puedan ser más eficientes dependiendo del cuadro genético del paciente. Un área en medicina conocida como farmacogenética. Sin embargo, estas investigaciones son solo ladrillos de un edificio que sigue en obra gris.
La importancia de ver la interacción entre nosotros y el COVID-19 con lentes genéticos puede aportarnos más información para comprender los síntomas y qué tan severa puede ser esta enfermedad. A esto le apunta el estudio de Coronagenes de la Universidad de Edimburgo, Escocia. “Queremos diseccionar la enfermedad en las partes más pequeñas que podamos, para ver si podemos reducir la complejidad que tiene”, explica Albert Tenesa, PhD en genética cuantitativa y uno de los investigadores principales de este proyecto.
Es evidente que este virus no afecta a todo el mundo por igual, ya se sabe que a cierta parte de la población puede llevarla a una unidad de cuidados intensivos, mientras que en otra pasa casi que desapercibido. Hay personas que no tienen síntomas, pero siguen siendo transmisores del virus. ¿Por qué pasa esto? “Entender si hay variaciones genéticas y, si es el caso, cuánta variación hay, podría ayudar a comprender mejor la enfermedad”, agrega Tenesa.
¿Por qué unas personas se enferman de COVID-19 y otras no? ¿Hay genes que influencian la gravedad de la enfermedad o cuánto puede durar? ¿Hay genes que también estén involucrados con otras enfermedades? Este el tipo de preguntas que quieren responder estudios como el de Coronagenes.
¿Y cuál es el plan? “Cerca de 30 millones de personas en el mundo se han hecho una prueba de ADN ancestral”, dice Tenesa. La información genética de pruebas ancestría que la gente se ha practicado, como las que ofrecen distintas empresas tipo 23andMe o Ancestry.com, son uno de los puntos de partida para este estudio.
Cabe mencionar que este tipo de pruebas pueden ser más precisas en poblaciones demográficas sobre las que ya hay un conocimiento previo de su ancestría, como las europeas o estadounidenses. Sin embargo, a la luz de encontrar información relevante que se pueda relacionar con enfermedades infecciosas, “es posible sacar información relacionada con la susceptibilidad genética de estos tipos de análisis”, comenta el médico Zarante al respecto. Además, existiría un ahorro de tiempo y recursos “pues solo habría que hacer análisis bioinformático con bases de datos”, agrega.
La gente que participe en Coronagenes debe completar un cuestionario sobre su estado de salud, estilo de vida, síntomas, datos demográficos, etc. Este estudio analizará y cruzará estos datos con la información de su ADN, y así, posiblemente, descubrir qué genes están involucrados con el riesgo de padecer COVID-19. Aquí, “las personas que han contraído la enfermedad son igual de importantes a las que no”, plantea la investigación. Los resultados que arrojen estos análisis serán de corte poblacional y no individuales.
En definitiva, las aproximaciones genéticas son migajas necesarias que hay que seguir para llegar a donde queremos: entender cómo funciona este coronavirus, por qué la enfermedad que produce tiene características tan particulares en distitos pacientes y en un futuro encontrar tratamientos que puedan ser más efectivos.
Los análisis genéticos no solo se hacen en nuestro genoma, también en la información genética del virus para rastrear cómo ha cambiado, a través de sus mutaciones, desde que que se descubriera a finales del 2019. Otro punto a favor de la genética.
Nuestro presente con este virus, y de hecho la historia humana, son la viva muestra de lo que plantearon teorías como la de Darwin y Mendel: intentar sobrevivir y heredar esas capacidades que lo permitieron. Los virus han dejado huellas profundas en la evolución de nuestra especie y la de otros mamíferos. Estas máquinas diminutas “buscan”, como nosotros, adaptarse al medio que habitan, por eso uno de los posibles escenarios es que, conforme pase el tiempo, y como ha pasado con otros virus y pandemias, la agresividad de ellos tienda a disminuir. O, como describe Ignacio Zarante, “No es otra cosa que una relación entre ambos genomas que tratan de “hacerse pasito” para que todos sobrevivamos”. Claro, mientras esto se da, habrá costos que, como humanidad, tendremos que asumir.
Efraín Rincón es biólogo y periodista científico. Ha escrito para diferentes medios como Cerosetenta, Pesquisa Javeriana o el Toronto Star, sobre ciencia y medio ambiente. Es coproductor de Shots de Ciencia, una plataforma de divulgación científica.
Las ilustraciones son de Lina Arias